 片頭痛とグルタミン酸 ― 新しい治療の可能性を探る
片頭痛とグルタミン酸 ― 新しい治療の可能性を探る
(原著:Khalsa N, Alves LB, Goadsby PJ. Glutamate as a therapeutic substrate for migraine. Int J Mol Sci. 2025;26(7):3023. https://doi.org/10.3390/ijms26073023)
背景
片頭痛は「ズキズキする頭痛」に加えて、光や音に敏感になる、吐き気を伴うといった症状を伴う一般的な神経疾患です。世界では10億人以上が悩まされているとされ、日常生活や仕事・家庭生活に大きな影響を与えます。最近ではCGRP(カルシトニン遺伝子関連ペプチド)を標的とした薬が登場していますが、それでも十分に効果が得られない患者さんが少なくありません。特に「前兆(閃輝暗点など)」を伴う片頭痛の患者さんには治療選択肢が限られています。
研究者たちは、脳内の主要な興奮性神経伝達物質である グルタミン酸 が、片頭痛発作の仕組みに深く関わっていることに注目しています。
目的
この論文の目的は、片頭痛におけるグルタミン酸の役割を整理し、グルタミン酸受容体を標的とした新しい治療法の可能性を明らかにすることです。特に、
-
グルタミン酸が関与する神経過敏(中枢感作)
-
前兆の原因となる皮質拡延性抑制(CSD)
-
痛みの伝達経路での役割
といった仕組みに焦点を当てています。
方法
研究チームは、既存の基礎研究・動物実験・臨床試験の文献を幅広くレビューしました。グルタミン酸受容体には大きく2種類あり、
-
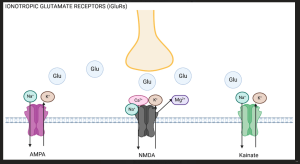
イオン型受容体(NMDA、AMPA、カイニン酸受容体):興奮性の神経伝達を担い、神経の過剰興奮に関与。
-
代謝型受容体(mGluR):神経活動の調整に関与し、痛みの感受性を上下にコントロールできる。
それぞれが片頭痛の発症や進行にどう影響するかを分析しました。
結果
レビューの結果、以下の点が明らかになりました。
-
グルタミン酸と痛み
三叉神経系や視床といった片頭痛に関わる脳の部位で、グルタミン酸は痛みの伝達や感作に重要な役割を果たしていました。 -
グルタミン酸と前兆
グルタミン酸は「皮質拡延性抑制(CSD)」を促進することがあり、これが前兆現象の原因と考えられています。特に遺伝性片頭痛の患者では、グルタミン酸伝達が過剰になりやすいことが示されています。 -
治療標的としての可能性
動物実験や初期の臨床研究では、NMDA受容体やmGluRを抑える薬が片頭痛症状を軽減する可能性が示されています。ただし、薬の副作用や効果の持続性、脳への薬剤到達といった課題が残されています。
結論
グルタミン酸は、片頭痛の「痛み」と「前兆」の両方に関わる重要な因子であり、グルタミン酸受容体を標的とした治療法は新しいアプローチとして有望です。特に、既存のCGRP標的治療で十分な効果が得られない患者さんにとって、新しい選択肢となる可能性があります。
今後は、受容体サブタイプごとの作用をより詳しく解明し、副作用を最小限に抑えた薬剤開発が進むことで、片頭痛治療の幅がさらに広がることが期待されます。
院長コメント
私自身もかつて「視覚とグルタミン酸による神経伝達」の研究に関わった経験があり、この分野には強い関心を持っています(末尾注)。片頭痛の「閃輝暗点」などの前兆は視覚領域に関連して起こることが多く、グルタミン酸の過剰な神経興奮と密接に結びついている点は非常に興味深いところです。
今後、神経科学の知見が臨床現場に届くことで、これまで十分な治療が難しかった片頭痛患者さんに新しい希望がもたらされるかもしれません。
📖 出典
Khalsa N, Alves LB, Goadsby PJ. Glutamate as a therapeutic substrate for migraine. Int J Mol Sci. 2025;26(7):3023. https://doi.org/10.3390/ijms26073023
末尾注; Unilateral eyeball enucleation differentially alters AMPA-, NMDA- and kainate glutamate receptor binding in the newborn rat brain
-
著者:M. Kiyosawa et al.
-
雑誌:Neurosci Res. 1996年11月;26(3):215‑24.
-
DOI:10.1016/S0168‑0102(96)01103‑0
-
概要:出生ラットにおいて、一側性の眼球摘出(enucleation)がNMDA、AMPA、カイネート型グルタミン酸受容体の結合に及ぼす影響を、視覚関連および非視覚関連脳部位で定量的に評価しています。
-
視覚関連部位では、PN20からPN30にかけてNMDAおよびカイネート受容体の結合が増加(例:上丘+45%、視覚皮質層IV+55%)、AMPAは安定。
-
摘出側ではアデノシンA1受容体の密度が大幅減少する一方、NMDAおよびAMPA受容体はわずかに増加。カイネート受容体はわずかながら減少。
-
このように、受容体サブタイプごとに時間経過および部位によって異なる変化が起こることを示唆しています。サイエンスダイレクト+8PubMed+8nichigan.or.jp+8
-




コメント