 清澤のコメント:リサーチゲートというサイトで我々の論文を読んで知らせてくれた方がいました。脳循環停止後の大脳視覚領の層状壊死による皮質網は早期にみた場合、原因が分かりにくいことがあります。FDG-PETでは視覚領の低下が明白にわかり、MRIに戻ってみると、その部分が層状壊死になっていることがわかるという20年前の短報です。この短報の後、しばらくこのような例の話が流行った気がします。
清澤のコメント:リサーチゲートというサイトで我々の論文を読んで知らせてくれた方がいました。脳循環停止後の大脳視覚領の層状壊死による皮質網は早期にみた場合、原因が分かりにくいことがあります。FDG-PETでは視覚領の低下が明白にわかり、MRIに戻ってみると、その部分が層状壊死になっていることがわかるという20年前の短報です。この短報の後、しばらくこのような例の話が流行った気がします。
ーーーーーーーー
短報:大動脈弓手術後の皮質盲(cortical blindness)
https://doi.org/10.1016/S0021-5155(01)00370-7
抄録
目的:大動脈弓手術中に計画された循環停止後に皮質失明が生じたマルファン症候群患者を報告する。
症例:31歳男性、マルファン症候群による急性大動脈解離のため大動脈弓手術を受けた。 彼は手術後に視力が低下していることに気づきましたが、瞳孔反射と眼底は正常に見えました。 手術後 2 年 9 か月後に磁気共鳴画像法 (MRI) と陽電子放出断層撮影法 (PET) が行われました。
結果: MRI では後頭皮質の皮質萎縮が明らかになり、フルオロデオキシ グルコースを用いた PET スキャンでは後頭皮質の極度のグルコース代謝低下が明らかになりました。 この萎縮は、おそらく手術中に計画された脳への循環停止中に起こった皮質層壊死を反映していた。
結論: MRI による皮質失明の診断は、特に急性期では困難な場合があります。 PETを使用すると、後頭皮質の顕著な代謝低下を見つけることができました。
この大脳皮質の層状壊死という言葉はつい最近でも解説が出ており、私たちの観察の正確さが確認できます。脳梗塞をこの概念と混同してはいけないと述べられていて、大脳皮質の第3層に弱いところがあるそうです。
◎ 皮質層状壊死(DOI:
最終改訂日: Henry Knipe、2023 年 9 月 12 日
偽層状壊死としても知られる皮質層状壊死は、酸素とグルコースの供給が地域の需要を満たすのに不十分な状況での脳皮質のニューロンの壊死です。 これは心停止、全体的な低酸素症、低血糖症でよく見られます。
これを、血栓塞栓性脳梗塞後に頻繁に起こる皮質内の固有の T1 高信号と混同しないでください 13。
用語
皮質層板壊死という用語は、ありふれた血栓塞栓性の「全層」脳梗塞後の数週間、数か月、または数年間における皮質 T1 固有高信号領域または皮質ジストロフィー性石灰化の領域を説明するときによく使用されます。 これは誤りであり、この用語が無意味になります。 13.
細胞レベルでの変化の根本的な理由はおそらく同じですが(つまり、単球の流入と細胞残骸の貪食による皮質を伴う液状壊死)、区別するのは細胞損傷の全体的なパターン(つまり皮質に限定される)です。 他のより局所的な虚血性損傷(例えば、血栓塞栓性脳梗塞)による皮質層壊死および偽層状壊死 10.
したがって、これらの用語は、たとえ同様の病理学的変化が梗塞の縁に見られたとしても、皮質下白質損傷が存在する血栓塞栓性梗塞の状況では使用されるべきではない13。むしろ、この用語は、 皮質の孤立した関与がある梗塞がある場合にのみ使用されるべきである。
さらに、皮質層状壊死と偽層状壊死はしばしば同じ意味で使用されますが、一部の出版物では区別を主張しています 9,10。 これが意味のある区別であるかどうかについてはおそらく議論の余地があるでしょう。
臨床所見
皮質層壊死または偽層壊死は、必要な機能に十分な栄養素を提供する脳の能力を損なう出来事を経験した患者に見られる傾向があります。 これは、供給の減少(例:低酸素症、虚血、場合によっては低血糖)または需要の増加(例:てんかん重積状態)のいずれかが原因である可能性があります11。
より具体的には、次の場所で発生します。
脳灌流低下
心停止または低血圧に続発して全身化する
関連する血管(通常は内頸動脈)の低血圧および狭窄による流域(境界領域)の分布
低酸素症
低血糖症
重度の貧血などの血液疾患
てんかん重積状態(脳がより多くのブドウ糖と酸素を要求するため)
シアン化物中毒12
病理学
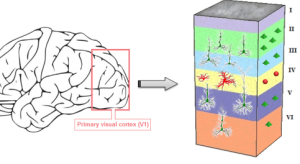
皮質層壊死は、皮質内のニューロンがグリア細胞や隣接する白質よりもはるかに代謝活性が高いために発生します。 さらに、大脳新皮質の特定の層は代謝ストレスや特定の脳領域(一次視覚野や陸地周囲皮質など)に対して選択的脆弱性があります。 3 番目の層が最も脆弱ですが、2 番目と 4 番目の層は虚血/低酸素に対してはるかに耐性があり、1 番目と 6 番目の層は中程度の脆弱性です13。
関与の分布は、回頭冠よりもむしろ溝の土手(側面)と基部を好む傾向があります13。
慢性期では、脳梗塞で見られるように、脳軟化症ではなく鉄沈着を特徴とする皮質下白質の関与が限定的である 13。
灰白質の選択的脆弱性は、代謝要求が高く、無酸素虚血事象後に放出される興奮性アミノ酸の受容体の濃度が高いことが原因である可能性があります。
X線撮影上の特徴
層状壊死は、無酸素虚血事象から数時間以内に特定される場合があります。 DWI は、急性期におけるこれらの皮質変化を区別するために、従来の MRI シーケンスよりも優れています 6。
CT
CT 上での皮質層壊死の外観は微妙であり、タイミングに応じて低密度と高密度の両方の減衰の回状変化として現れます。 明らかな出血や石灰化はありません。 数日後、脊椎の強化が見られ、通常は最大 3 か月間持続します。
MRI
初期の細胞傷害性浮腫は、影響を受けた皮質で対応する低い見かけの拡散係数(ADC)値を伴う高信号を DWI で引き起こし、皮質の増強は後で、通常は 2 週間後に見られる可能性がありますが、固有の T1 信号の増加が最も特異的な画像特徴です。
層板壊死を知らせる T1 曲線状の高信号は、脳卒中後 3 ~ 5 日ほどで明らかになりますが、通常は 2 週間後、強度のピークは約 1 か月で、その後ゆっくりと消えていき、通常 6 ~ 8 か月ほどで徐々に消えていきます。 場合によっては、侮辱後 1 年以上目に見える状態が続くこともあります 7,8。 この T1 高シグナルは、瀕死の細胞および/または脂質を含んだマクロファージにおける変性タンパク質の蓄積によって引き起こされると考えられています。 重要なことは、これは出血やカルシウム 6、7、13 の存在を示すものではないということです。




コメント