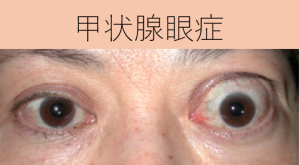
 新しい甲状腺眼症治療薬テッペーザの有用性と忍容性について 廣松雄治(久留米大名誉教授)
新しい甲状腺眼症治療薬テッペーザの有用性と忍容性について 廣松雄治(久留米大名誉教授)
清澤の聴講印象記
第38回甲状腺眼症研究会(2025年3月22日 日本青年館ホテル):
講演では、テッペーザ(一般名はテプロツムマブ)の有効性が語られました。この製剤も他の生物学的製剤と同様に、1本の価格が100万円もし、2度目の投与からは2本を要するため、初年度の薬剤費が1000万を超えることになります。現在は高額医療費補助があるにもかかわらず、本人の支払額は無視できないものであり、更に治療した患者の2~3割には再発も見られるそうです。このような状況下で、演者は治験を主導しましたが、甲状腺眼症治療の主流がすぐにテプロツムマブに移行すると考えているわけではないようでした。
—
講演要旨から抜粋
甲状腺眼症は、高頻度でパセドウ病に合併する眼窩組織の自己免疫性炎症性疾患です。わが国では2011年に「バセドウ病悪性眼球突出症の診断基準と治療指針」が公開され、2023年には第3次案(注1)が提示されました。この指針では、内科医と眼科医の連携、およびMRIによる病勢の把握に基づいた適切な治療法の選択が推奨されています。
中等症から重症の活動性眼症患者には、メチルプレニゾロン・パルス療法が第1選択の治療法として推奨されてきました。しかし、保険適応外使用であることや、副作用に対する対応が必要であることから、利用できる施設が限られていました。また、眼球突出に対する効果が十分ではなく、慢性期には手術療法が必要なケースも多く、課題が指摘されていました。
2023年12月に行われた甲状腺眼症に対する第Ⅲ相臨床試験では、テプロツムマブの有用性と安全性が確認され、2024年9月に医薬品医療機器総合機構(PMDA)より製造販売が承認され、同年11月に「テッペーザ®」として発売されました。
Teprotumumab(テプロツムマブ)について:テプロツムマブは、ヒト型抗インスリン様成長因子-1受容体(IGF-1R)モノクローナル抗体であり、IGF-IRの下流のシグナル伝達を阻害します(注2)。特に眼球突出に顕著な効果を示し、活動性甲状腺眼症の治療選択肢が増えることで、診療アルゴリズムが大きく変化する可能性があります。
講演では、わが国で行われた第Ⅲ相臨床試験を中心に、海外データも含めたテプロツムマブの有効性と忍容性について紹介され、甲状腺眼症の診断と治療の現状、及び今後の展望が概説されました。
【わが国で行われた Teprotumumab の臨床試験】
日本人の活動期中等症~重症の甲状腺眼症患者を対象とした第3相臨床試験において、テプロツムマブは以下の成績を示しました:
– **眼球突出の改善**:24週目で89%の患者に>2mmの改善
– **CASスコアの改善**:59%の患者がCAS 0~1点に改善
– **複視の消失**:50%の患者で複視が消失
副作用として高血糖(22%)と聴覚障害(15%)が報告されましたが、重篤な副作用は認められず、忍容性も良好でした。
注1
バセドウ病悪性眼球突出症(甲状腺眼症)の診断基準と治療指針2023 (第3次案) 日本甲状腺学会・日本内分泌学会 臨床重要課題「バセドウ病悪性眼球突出症の診断基準と治療指針の作成」委員会:で検索可能です。
注2
テプロツムマブは、IGF-1Rの下流シグナルを阻害し、炎症と免疫反応を抑える作用を持ちます。眼窩組織の腫れや繊維化を改善し、眼球突出や視覚症状の緩和に寄与します。
注3
甲状腺眼症(TED)の評価に用いられるCAS(Clinical Activity Score)は、疾患の活動性を客観的に判断するスコアシステムです。炎症や浮腫に関連する7項目で評価され、それぞれの項目を1点として合計し、3点以上を活動性眼症として判断する基準が一般的です。




コメント