 清澤のコメント:この文は先のミニレビューの中から神経伝達物質の項目を抜粋して翻訳したものです。これを読むと、一見関連のないリボトリールとアーテンが共に眼瞼痙攣患者の症状を一時的にせよ変化(軽減)させる効果を持ちうるのかが推測できます:
清澤のコメント:この文は先のミニレビューの中から神経伝達物質の項目を抜粋して翻訳したものです。これを読むと、一見関連のないリボトリールとアーテンが共に眼瞼痙攣患者の症状を一時的にせよ変化(軽減)させる効果を持ちうるのかが推測できます:
5 神経伝達物質
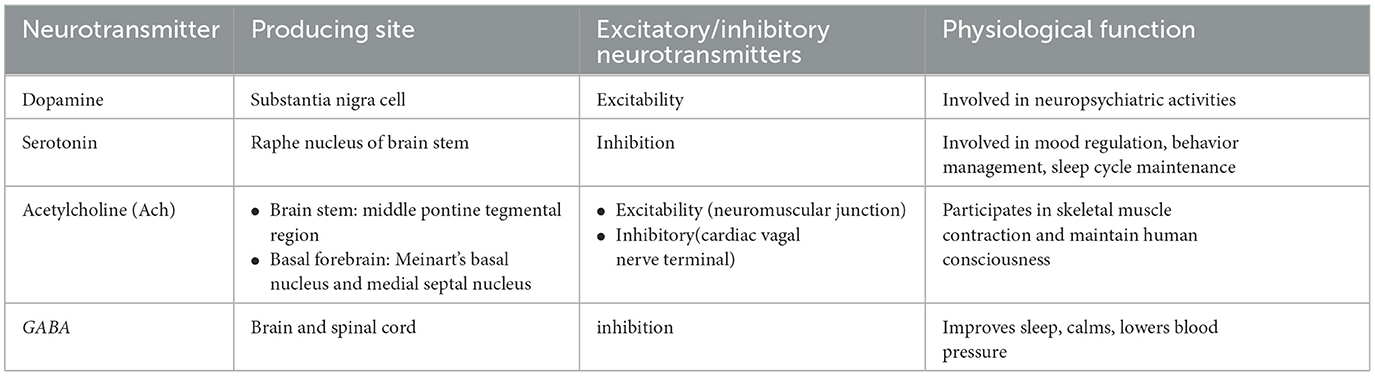
眼瞼けいれんの正確な病因は完全には解明されていませんが、いくつかの研究では、眼瞼けいれんがドーパミン受容体過敏症、コリン作動性神経系の過剰活動、γ-アミノ酪酸(GABA)機能不全など、さまざまな神経伝達物質系の機能不全に関連している可能性があることが示されています(4、80 – 82 ) (表 1 ) 。
5.1 ドーパミン
ドーパミン (DA) は、ジストニアに関与する主要な神経伝達物質の 1 つであると考えられています。筋肉の緊張を維持し、人体の随意運動を調節する上で非常に重要な役割を果たします。ドーパミン神経支配の微妙な異常は眼瞼けいれんの素因であり、これが生理学的にドーパミンが減少している高齢者に眼瞼けいれんがより多く発生することを説明している可能性があります( 83 )。しかし、ドーパミン作動系がジストニアの病態生理学に関与する正確な機構は依然として不明です( 84 )。眼瞼けいれんの原因は、ドーパミン受容体の減少によって引き起こされる、ドーパミンまたはその他の神経伝達物質の代謝経路の異常である可能性があるという仮説が立てられています(図1)。例えば、ドーパミンアゴニスト(レボドーパ、ブロモクリプチンなど)などの特定の薬物は、黒質線条体GABA作動性ニューロンの機能低下を引き起こし、それによってドーパミン作動性受容体過敏症を引き起こし、中枢ドーパミン作動性を増加させるため、眼瞼けいれんを誘発する可能性があります( 4、82 ) 。活動が低下し、頸顔面ジストニアを引き起こします。
清澤注:このレビュー論文には、次の我々の論文がこの引用から漏れていると思います。
Decreased dopamine D2 receptor binding in essential blepharospasm
ーーーーーーー
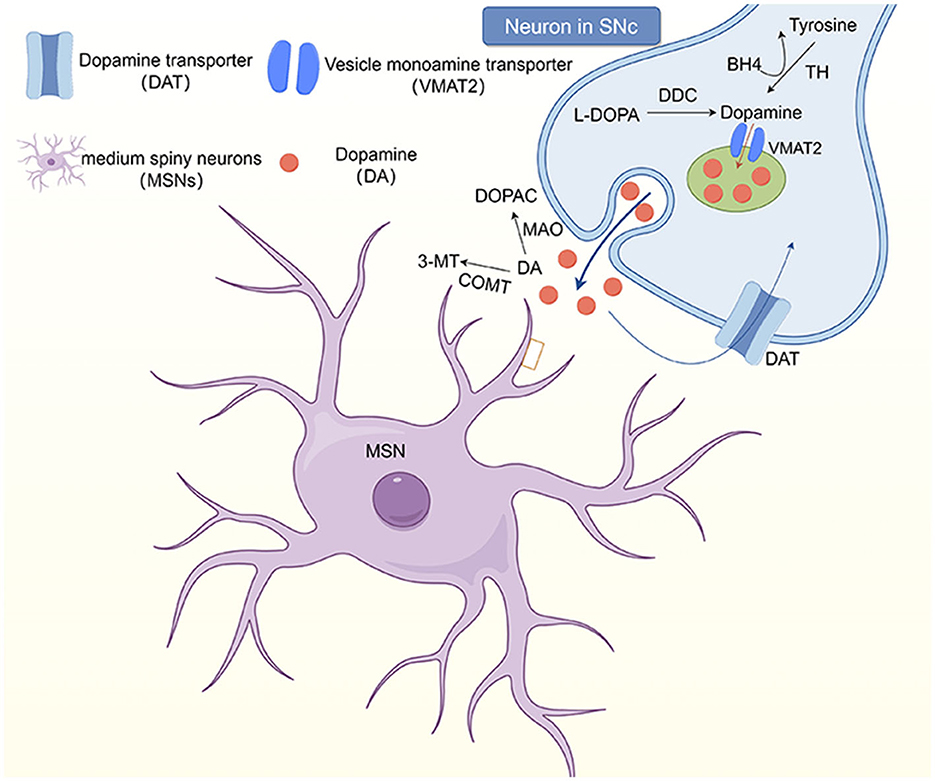
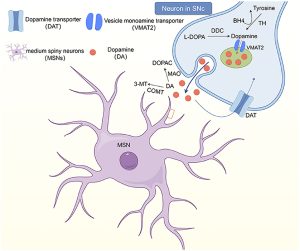
図1。線条体のドーパミン作動性システム。黒質部黒質 (SNc) のニューロンは、線条体経路を通じてドーパミン作動性入力を受け取ります。シナプスレベルでは、チロシンヒドロキシラーゼ(TH)はテトラヒドロビオプテリン(BH4)を補因子として使用してチロシンに変換し、シナプス前末端でドーパミンを合成します。ドーパミン(DA)および他のモノアミンは、小胞モノアミン輸送体(VMAT2)によってシナプス前末端の小胞に導入されます。ただし、モノアミンはシナプス ギャップに放出され、ドーパミン受容体 (D1 ~ 5) を含むシナプス後受容体に結合します。シナプスギャップの DA は、モノアミンオキシダーゼとカテコールオキソメチルトランスフェラーゼ (COMT) によってそれぞれ 3,4-ジヒドロキシフェニル酢酸 (DOPAC) と 3-メトキシチラミン (3-MT) に分解され、シナプス前末端に輸送されます。
ーーーーーー
線条体のドーパミンレベルの変化は、直接的および間接的な線条体 – 淡蒼球経路の不均衡を引き起こす可能性があります ( 85 )。投射ニューロン (SPN) は線条体の主要な細胞タイプであり、直接的および間接的な線条体 – 淡蒼球経路の起源となります。SPN は、線条体から外淡蒼球 (GPe)、内淡蒼球 (GPi)、および黒網様体 (SNr) 領域に投影します。SPN から GPi および SNr への投影は「直接経路」であり、GPe への投影は「間接経路」です。ドーパミンはドーパミン受容体 D1R と D2R の活性化を誘導し、これらは直接的および間接的な線条体 – 淡蒼球経路に反対の効果をもたらします。過剰運動は、線条体 – 淡蒼球の直接経路が適切に刺激されると発生しますが、重度の運動能力低下は、間接的な線条体 – 淡蒼球経路が刺激されると発生します。リボットらは( 84 ) 線条体中のドーパミンが直接的および間接的な線条体-淡蒼球経路間のバランスを厳密に制御することによってさまざまなジストニア表現型を説明するという推定モデルを提案した。
DA の代謝産物である 3-メトキシチラミン (3-MT) は、新しく認識されたタイプの神経調節物質であり、場合によっては運動制御に関与している可能性があります ( 86 )。脳内の 3-MT の濃度は、カテコール-O-メチルトランスフェラーゼ (COMT) ( 87 ) およびモノアミンオキシダーゼ (MAO)、主に MAO-A ( 88、89 )の活性によって厳密に制御されています。COMT 活性の増加または MAO 活性の減少は、3-MT 濃度の増加につながります。中心的な COMT 媒介ドーパミン代謝産物 3-MT は、微量アミン関連受容体 1 と相互作用することで運動に影響を与えます ( 89 )。我々は、3-MT 上昇が眼瞼けいれんと密接に関連している可能性があると推測しています。Timmersらによって行われた研究で( 85 )は、対照と比較して、けいれん性斜頸症、ドーパ反応性ジストニア(DRD)、およびミオクローヌスジストニアの患者において、より高い3-MTレベルを観察した。現在の研究では、ジストニア患者におけるドーパミン作動性の変化が実証されています。私たちの研究はまた、血漿カテコールアミンを使用してジストニア患者の3-MT異常を実証した最初の研究でもあり、ジストニアの病因についてのより包括的な証拠を提供します。したがって、利用可能な研究に基づいて、我々は 3-MT の上昇をジストニアのバイオマーカーとして提案します。将来的には、ジストニア患者についてさらに詳しく研究する必要があります。
5.2 セロトニン
中枢神経系では、セロトニンは脳幹の正中線に位置する縫線核内のニューロンによってほぼ完全に生成されます ( 90 )。ウォールマンら( 91 ) は、背側縫線核 (dRN) とそのセロトニン作動性ニューロンが大脳基底核と感覚運動皮質に接続されていることを発見しました。大脳辺縁系で高度に発現するセロトニンは、神経活動および神経心理学的プロセスを調節する感情調節因子である可能性があるため、市場の関心を集めている神経伝達物質です。精神障害におけるその役割は広く研究されており ( 92 )、セロトニン作動系の調節不全は多くの精神障害および神経障害の発症に関連しています ( 90、93、94 )。
セロトニン系は、ジストニア患者では 5-ヒドロキシインドール酢酸 (セロトニンの主要代謝産物) のレベルが低下するという点でジストニアに関連しています ( 95 )。ティマーズらは、ジストニア患者のトリプトファン (セロトニンの前駆体) 濃度が健康な人よりも著しく低いことを発見しました ( 85 )。現在、ほとんどの形態のジストニアに対して有効な治療選択肢はありません。選択的セロトニン作動薬に関するさらなる研究は、ジストニアの新しい治療法の開発につながる可能性があります。
5.3 コリン作動性神経系
線条体におけるドーパミンとアセチルコリンの間の相互作用は、ジストニアの重要な原因です。アセチルコリンは線条体のドーパミン神経伝達に強力な影響を及ぼし、運動学習において重要な役割を果たしていることが示されています ( 96 )。アセチルコリンアゴニストは眼瞼けいれんを誘発する可能性がありますが、抗コリン薬(例、ベンゼドリン)は線条体におけるドーパミンの放出に影響を及ぼし、それによって眼瞼けいれんを改善します。新しい文献の多くは、随意運動および運動障害の臨床症状の制御におけるコリン作動性伝達の中心性を強調している( 97 )。
5.4 GABAギャバ
以前の研究では、線条体、一次および運動前野、体性感覚皮質、および小脳における GABA-A 受容体の機能不全がジストニアの発症と関連している可能性があることが示唆されています( 98、99 )。クロナゼパムは、GABA の放出と伝達を促進するベンゾジアゼピン受容体作動薬であり、ベンゾジアゼピンの長期使用は脳内の GABA 受容体の下方制御を引き起こし、場合によっては眼瞼けいれんを引き起こす可能性があります ( 76 )。鈴木ら( 100 ) は、異常な GABA 機能が眼瞼けいれんの発生と関連している可能性があることを示唆しました。フォルステラらは( 101 ) エタノールが脳内の GABA 作動性神経伝達を強化することを発見しました。これは、なぜアルコール摂取が眼瞼けいれんのリスクを軽減するのかを説明しています。
ーーーーーーーー
健康長寿医療センターにおける我々の研究の報告書(石井の報告書)リンク;chrome-extension://efaidnbmnnnibpcajpcglclefindmkaj/https://kaken.nii.ac.jp/ja/file/KAKENHI-PROJECT-20591038/20591038seika.pdf




コメント