清澤のコメント:夜盲や視野における輪状暗点を示す進行性の疾患である網膜色素変性症は、日本人の失明原因(視覚障害の指定を受けた患者における割合)の第3位であり利用可能な治療法の確立が強く求められている疾患です。しかし、網膜色素変性症におけるRP65遺伝子変異を持つ症例の割合については、日本人では非常にまれです。¹ RP65遺伝子は、網膜の視細胞でレチノールをレチナールに変換する酵素をコードする遺伝子で、この過程は視覚サイクルの一部です。RP65遺伝子に変異があると、視細胞が光を感知できなくなり、網膜色素変性症の一種であるロイシン-リッチリピートネクチンタイプ1(LRAT)欠損症を引き起こします。²RP65遺伝子変異を持つ症例は、欧米では約0.5%の割合で報告されていますが、日本人ではこれまでにわずか2例しか報告されていません。³ したがって、日本人の網膜色素変性症患者の中でRP65遺伝子変異を持つ割合は0.02%未満と推定されています。
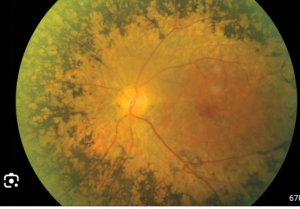 Gene therapy for RPE65-mediated inherited retinal dystrophy completes phase 3 – The Lancet
Gene therapy for RPE65-mediated inherited retinal dystrophy completes phase 3 – The Lancet
ソース:(1) 2022 年11 月14 日 日本人における遺伝性網膜疾患の遺伝的特徴. https://tokyo-mc.hosp.go.jp/wp-content/uploads/2022/11/pressrelease_20221114.pdf
(2) 長鎖シークエンスにより網膜色素変性の原因遺伝子変異を解明 …. https://www.amed.go.jp/news/release_20220616-02.html
(3) 公益社団法人日本網膜色素変性症協会 | Japanese Retinitis …. https://jrps.org/
ーーーーーーーー
厚労省 遺伝性網膜ジストロフィーの遺伝子治療薬・ルクスターナを承認
公開日時 2023/06/27 04:50
厚生労働省は6月26日、ノバルティスファーマの遺伝性網膜ジストロフィー(IRD)に対する遺伝子治療薬・ルクスターナ注(一般名:ボレチゲン ネパルボベク)を承認した。投与対象は、遺伝学的検査によりRPE65遺伝子の両アレル性の変異が確認されたIRD患者となる。各眼の網膜下に単回投与する。
遺伝子治療薬としてはコラテジェン筋注用、ゾルゲンスマ点滴静注、デリタクト注に続く4製品目で、眼科領域の遺伝子治療薬は初となる。8月ごろにも中医協で保険償還価格が決まる見通し。
ルクスターナの効能・効果は、「両アレル性RPE65 遺伝子変異による遺伝性網膜ジストロフィー」。再審査期間は10年。
ルクスターナはIRDの原因遺伝子の1つであるヒトRPE65遺伝子を搭載した非増殖性組換えアデノ随伴ウイルス(AAV)を成分とする再生医療等製品。網膜下にある網膜色素上皮(RPE) 細胞に感染することにより、搭載された遺伝子発現構成体が細胞の核内にエピソームとして留まり、ヒトRPE65遺伝子は長期間安定して発現する。RPE65遺伝子の機能欠損を補い、発現したRPE65タンパク質により正常な視覚サイクルを回復させることで、視覚機能の改善効果を期待する。
用法・用量または使用方法は「通常、1.5×1011 ベクターゲノム(vg)/0.3mLを各眼の網膜下に単回投与する。各眼への網膜下投与は、短い投与間隔で実施するが、6日以上あけること。同一眼への本品の再投与はしないこと」となっている。




コメント