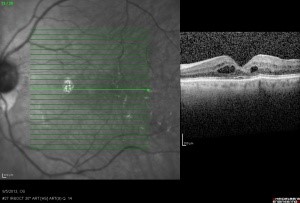
嚢胞様黄斑浮腫とは:
清澤のコメント:CMEは眼科臨床医にとって一見理由の解らない視力低下の原因であることが多い疾患です。OCTで網膜断層像を見ればその存在は比較的容易に見出せます。内科的ないし外科的治療につなげてやればよいでしょう。OCTで区別できますが、基幹病院に紹介する際には中心性漿液性網脈絡膜症との鑑別はしっかりつけておきたいです。⇒嚢胞様黄斑浮腫(のうほうようおうはんふしゅ)【CME】は、目の中で拡張した毛細血管から血漿成分の漏出がおこり、網膜の中心である「黄斑」という部分に液体貯留をしてしまう病気です。 液体が貯留してしまうことにより浮腫を生じ、進行した場合、嚢胞様黄斑浮腫といいます。
―――元記事の要点です―――――
割り当てられたエディター:Diana V. Do、MD
レビュー:2019年
嚢胞性黄斑浮腫
病気の実体
疾患
米国眼科学会の優先診療パターンでは、嚢胞性黄斑浮腫(CME)を、正常な血液網膜関門の破壊による黄斑の網膜肥厚と定義しています。これにより、中心窩周囲の網膜毛細血管からの漏出と、網膜の細胞内空間、主に外網状層内の体液の蓄積が引き起こされます。視力喪失は、光受容体の構造を歪める網膜の肥厚と体液の収集から発生します。CMEは、先進国における中心視力喪失の主な原因です。
病態生理学
さまざまな危険因子が、網膜環境に影響を与える通常の相互作用を混乱させる可能性があります。網膜が破壊されると、不均衡が発生し、網膜の内層、最も一般的には外網状層(OPL)内の嚢胞状空間に体液の蓄積が見られます。液体の蓄積は通常、ヘンレの線維層で発生し、古典的な花弁状のパターンを引き起こします。
CMEを引き起こす可能性のある一般的な要因は硝子体牽引(VMT)です。VMTは、ミュラー細胞のエンドフィートにストレスを引き起こし、牽引力を発揮し、塩基性線維芽細胞増殖因子(bFGF)、血管内皮増殖因子(VEGF)、血小板由来増殖因子(PDGF)などの炎症性因子の放出に寄与します。
診断
サイン
細隙灯または直接/間接検眼鏡を使用すると、臨床的に重大な中心窩浮腫および300μmを超える網膜肥厚が中心窩反射の喪失として見られます。無症候性中心窩浮腫は300μm未満の浮腫として説明されています。
症状
症状には、網膜浮腫に関連する視力の低下、コントラスト感度と色覚の喪失、アムスラーグリッドで示される変視症、小視症、および中心暗点が含まれます。
危険因子
| 糖尿病 | 糖尿病性黄斑浮腫(DME)は、微小動脈瘤および網膜毛細血管からの漏出に関連しており、硬性滲出液またはリポタンパク質沈着物の循環リングを引き起こします。 |
| エピネフリン | エピネフリン滴で治療された無水晶体眼の28%に対して、未治療の無水晶体眼の13%がCMEを発症した |
| Pars Planitis / Uveitis | 扁平上皮炎では、CMEに関連するインターフェロンガンマ、インターロイキン-2などのT細胞炎症メディエーターの蓄積がある。 |
| 網膜色素変性症 | 通常、局所ドルゾラミドまたは全身アセタゾラミドに反応します。 |
| アーバイン-ガス | Irvine-Gassは、眼内レンズによる白内障摘出の最大20%で発生する炎症過程です。CMEは通常、術後6〜10週間で発生し、Irvine-GassによるCMEの95%は、6か月以内に自然に解消することが示されています。 |
| 静脈閉塞症 | 網膜中心静脈閉塞症/ CRVOと網膜静脈分枝閉塞症の両方がCMEを引き起こす可能性があり、これは通常、抗VEGF剤によく反応します。 |
| E2-プロスタグランジン | E2-プロスタグランジンは、網膜毛細血管の密着結合の破壊を引き起す。 |
| ニコチン酸とニコチン | CMEに関連するかすみ目が1.5g /日を超える用量で報告されている。 |
| 手術 | さまざまな種類の手術が炎症を引き起こし、網膜の血流を変化させる可能性がある。毛様体扁平部硝子体切除術(PPV)、レーザー光凝固術、クリオペキシー、緑内障の手術 |
イメージング
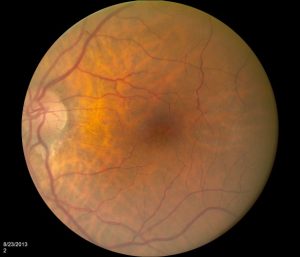
カラー眼底写真(CFP)は、ハニーコームパターンでヘンレ層の黄斑の中心窩領域内の網膜内嚢胞を示す(図1)。(図2は略)
フルオレセイン血管造影(FA)は初期段階では、中心窩周囲領域の毛細血管拡張が認められる。FAの後期(5〜15分)では、嚢胞状空間への漏出がヘンレ層に放射状に分布し、古典的な花弁状漏出パターン外観を形成します(図3)。
FFAは、視神経乳頭の後期での染色を示すこともあります(特に中等度ブドウ膜炎、アーバインガス症候群、バードショット脈絡網膜症)。漏出が周辺網膜や視神経の近くなど、他の場所にある場合、外観はよりハチの巣状に見えます。
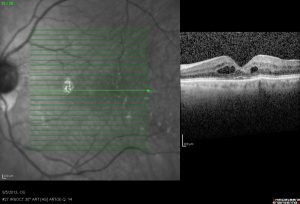 光コヒーレンストモグラフィー(OCT)は、網膜の断面の高解像度画像を客観的に取得します。CMEでは、OCTは、OPLで反射率の低い網膜内嚢胞性領域を描写することで網膜肥厚を測定することで診断できます[(図4)。
光コヒーレンストモグラフィー(OCT)は、網膜の断面の高解像度画像を客観的に取得します。CMEでは、OCTは、OPLで反射率の低い網膜内嚢胞性領域を描写することで網膜肥厚を測定することで診断できます[(図4)。
OCTは、網膜の内面にある過反射バンドを介して、VMTや網膜上膜(ERM)などの硝子体黄斑界面の異常によって誘発される機械的な力を表すことができます。重度のCMEでは、中心窩下液がOCTで明らかになることがあります。
自家蛍光(AF)は、RPEの状態を示し、網膜内嚢胞は自家蛍光増強として現れます。
網膜厚さアナライザー(RTA)は、網膜の広い3Dマップを生成します。
管理
一般的な治療
CMEの治療における治療的アプローチは、内科的であれ外科的であれ、根底にある病因に依存しています。ほとんどの場合、3〜4か月以内に減弱します。CMEが持続する場合は、医学的または外科的治療が必要です。
内科療法
NSAIDS –局所または全身のインドメタシンは、プロスタグランジンの産生を減少させるシクロオキシゲナーゼ酵素を阻害します。ケトロラクトロメタミン0.5%、インドメタシン1%、ネパフェナク0.1%、ブロムフェナク0.07%、およびジクロフェナク1%は、術後に無水晶体または偽水晶体のるCMEに使用されます。
コルチコステロイド–局所、眼周囲、全身、硝子体内注射またはインプラントコルチコステロイドは、ホスホリパーゼA2を阻害し、その結果、プロスタグランジンおよびロイコトリエンの産生を阻害します。ステロイドは特に黄斑浮腫に役立ちます。硝子体内トリアムシノロンは、ミュラー細胞の内因性アデノシンシグナル伝達を刺激し、VEGF産生を減少させることによって体液蓄積を減少させます。現在、4つのコルチコステロイドベースの硝子体内インプラントがあります(略)。ステロイド注射のよく知られた副作用には、緑内障と白内障が含まれます。トリアムシノロンアセトニドは、硝子体内、テノン嚢下、眼球周囲/中隔横断/眼窩底のさまざまな経路で投与できます。
炭酸脱水酵素阻害剤(CAI)– CAIは、RPEのイオン輸送システムの極性を変化させ、液体を細胞内空間から遠ざけます。CAIは、パクリタキセルおよびドセタキセルによって誘発されるCME およびRPによって誘発されるCME 役立ちます。
抗VEGF剤–ペガプタニブ(抗VEGF 165 RNAアプタマー)、ラニビズマブ(抗体フラグメント)、およびベバシズマブ(完全抗体)は、破壊された内皮細胞からの血管透過性を低下させることによって作用します。網膜の厚さと体液の蓄積の著しい減少がさまざまな研究で指摘されており、副作用が最小限に抑えられて視力が大幅に改善されています。
薬理学的硝子体溶解剤–コンドロイチナーゼ、ジスパーゼ、ヒアルロニダーゼ、プラスミン、およびマイクロプラスミンは、後部硝子体剥離を誘発して、CMEをVMTから解放します。マイクロプラスミンは現在、その安定性、患者の耐性、および保管と投与の容易さで最大の可能性を示す薬剤です。第II相試験では、125μgの用量を3回繰り返すと、注射の1か月後に58%の患者でVMTが放出されることが示されています。(略)
手術
PPVは、特に内科的治療に抵抗性がある場合に、牽引性または非牽引性の成分による黄斑浮腫を緩和するのに役立ちます。硝子体切除後の視覚的転帰の統計的に有意な改善を示しました(硝子体切除術-無水晶体-嚢胞性黄斑浮腫研究)。
牽引成分は、VMTで後部硝子体を放出するか、ERMの内境界膜剥離を行うことで対処できます。具体的には、糖尿病に続発するCMEを引き起こすVMTの牽引成分のPPVは、患者の80〜92%で黄斑浮腫を改善することが示されています。糖尿病、網膜中心静脈閉塞症(CRVO)、ブドウ膜黄斑浮腫、およびRPに続発するCMEの内境界膜剥離は解剖学的改善を示していますが、視力の結果は決定的ではありません。YAGレーザーは、虹彩への硝子体癒着などの牽引成分を軽減するのにも役立ちます。
非牽引性の要素は、PPVを受けたときに炎症性因子を理論的に取り除くことによって対処されます(略)。しかし、ある研究では、網膜静脈分枝閉塞症(BRVO)患者のVEGFレベルの上昇が、硝子体切除後の視力の改善と相関していることが示されました(略)。硝子体切除術の副作用には、白内障、網膜剥離、硝子体出血、および眼圧の上昇が含まれます。
予後
CMEは通常自己制限的であり、3〜4か月以内に自然に解消します。病因に応じて、浮腫の解決は、医学的または外科的オプションを介して支援される場合があります。浮腫が慢性的(6〜9か月以上)な場合、網膜の菲薄化と線維症を伴う光受容体への永続的な損傷が発生する可能性があります。
追加リソース
- ポーターD、ベムラコンダGA。黄斑浮腫。アメリカ眼科学会。EyeSmart ®目の健康。https://www.aao.org/eye-health/diseases/macular-edema-5。2019年3月18日にアクセス。




コメント